

发布时间:2026-03-31
3月26日,中国科学院广州生物医药与健康研究院联合美国约翰霍普金斯大学、重庆医科大学,在Advanced Science发表题为Reduced Maintenance DNA Methylation Thresholds Enable Sensitive Reporter Assays for UHRF1 and DNMT1 Inhibition的研究论文。该研究揭示了DNA甲基化维持蛋白UHRF1和DNMT1在调控DNA甲基化过程中存在显著的“高阈值效应”,并据此建立了靶向UHRF1-DNMT1调控轴的高灵敏度细胞水平筛选体系,为DNA甲基化干预药物的发现提供支撑。
DNA甲基化异常是驱动恶性肿瘤和多种遗传性疾病发生发展的关键表观遗传机制。异常DNA甲基化状态主要由DNA甲基转移酶DNMT1及其招募蛋白UHRF1共同维持,因此,UHRF1-DNMT1调控轴是DNA甲基化干预药物研发的重要靶标。尽管核苷类DNA甲基化抑制剂已获批用于血液肿瘤治疗,但此类药物存在毒性大、治疗窗口窄、易耐药等问题,限制了其临床应用。过去20余年间,非核苷类DNA甲基化抑制剂研发持续受到关注,但相关药物迄今尚未获得临床批准,其中一个重要原因是缺乏灵敏、高通量且适用于细胞水平化合物在靶(on-target)效应评价的药物筛选体系。
研究团队系统分析了UHRF1和DNMT1在维持DNA甲基化中的剂量需求,发现二者在细胞内具有较强的功能冗余性:肿瘤细胞仅需正常水平10%~20%的UHRF1或DNMT1蛋白,即可维持全基因组DNA甲基化状态;只有当其活性被抑制超过80%~90%时,才会出现显著的去甲基化和抑癌基因再激活。研究人员将这一现象概括为DNA甲基化维持的“高阈值效应”。这一效应使许多具有一定活性的苗头化合物在传统细胞筛选模型中难以被有效识别,从而制约了DNA甲基化干预药物的发现效率。
针对这一瓶颈,研究团队提出“遗传学干预促进化学干预”策略:通过基因编辑去除冗余的DNMT1或UHRF1蛋白,仅保留维持甲基化所必需的最低水平,从而提高细胞对活性化合物的响应敏感性。在此基础上,团队分别构建了DNMT1和UHRF1部分敲除的细胞模型,并将荧光素酶NLuc插入被DNA甲基化沉默的内源性抑癌基因位点,建立了用于筛选DNMT1和UHRF1抑制剂的细胞水平报告基因系统。结果表明,该体系可有效缓解“高阈值效应”,将筛选系统的灵敏度和动态范围提升50-200倍。
进一步地,研究团队对包含7000余种已知活性化合物的化合物库开展高通量筛选,证实该体系能够高效、特异地反映DNMT1和UHRF1抑制剂的在靶作用效果。团队还提出“先诱导DNA去甲基化、再序贯联合组蛋白修饰抑制剂”的用药策略,并证明该方案具有更优的抑癌效果,为表观遗传药物联合应用提供依据。
DNA甲基化是维持细胞谱系身份和调控细胞命运转换的重要表观遗传基础。靶向其异常调控,不仅有望纠正病理性基因表达失衡,还可从细胞命运重塑层面实现对异常细胞谱系的精准干预。该研究为开发具有细胞谱系重塑与干预潜力的新型DNA甲基化抑制剂提供方法学支撑。
广州健康院孔祥谦研究员、美国约翰霍普金斯大学Stephen Baylin教授和重庆医科大学郭祖奉教授为论文共同通讯作者。广州健康院与中国科学技术大学联合培养博士生夏翠翠为论文第一作者。该研究还得到广州健康院巫林平研究员、王杰研究员、黄靖副研究员、王丹阳博士以及美国Van Andel研究所Scott Rothbart教授的支持和帮助,并获得广州健康院抢占科技制高点重大项目、中国科学院战略性先导科技专项、广州国家实验室重大研究计划和国家自然科学基金等支持。
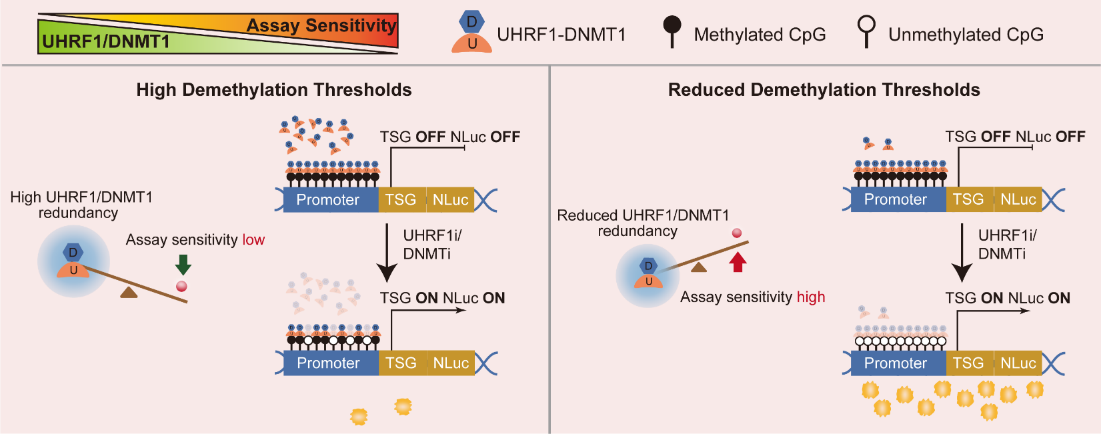
图1 降低UHRF1/DNMT1冗余表达,下调DNA甲基化维持阈值,提升细胞对DNA甲基化抑制剂的响应敏感性
附件下载:



