

发布时间:2026-03-31
近日,中国科学院广州生物医药与健康研究院蛋白修饰研究组、细胞器与干细胞研究组与多单位合作在 Cell Reports 期刊上发表了题为 “MAP2K6 directly phosphorylates BCL2L13 to mediate mitophagy for suppressing tumorigenicity” 的论文。该研究发现MAPK信号通路二级激酶MAP2K6可以定位在线粒体和自噬体上,通过磷酸化线粒体自噬受体BCL2L13的S426位点(BCL2L13-S426),增强其与LC3B的结合,进而促进线粒体自噬,抑制肺腺癌的发生。本工作揭示了由激酶MAP2K6介导的在细胞器互作界面上调控线粒体质量控制并重塑线粒体代谢的新机制,该机制在肺腺癌发生中发挥关键作用。
MAPK信号通路广泛参与生物发育及肿瘤发生过程。目前,其三级激酶p38、ERK1/2和JNK1的功能与其亚细胞定位已被报道,但是上游二级激酶MKK1-7的亚细胞定位与其具体功能之间的关系目前仍不清楚。
研究团队基于超高分辨成像技术,发现在MAP2K1-7这七种二级激酶中仅有MAP2K6与MAP2K3能够定位于线粒体及自噬体相互作用区域,表现出独特的亚细胞器定位特征。进一步研究表明,MAP2K6/MAP2K3可显著激活线粒体自噬,从而有效抑制肺腺癌的生长。在机制研究方面,团队发现MAP2K6抑制肺腺癌生长的功能依赖其激酶活性,但是并非通过其经典下游靶点p38。通过磷酸化修饰组学分析,发现MAP2K6可以直接磷酸化BCL2L13的S426位点,该位点的磷酸化修饰增强了BCL2L13与LC3B的相互作用,进而促进线粒体自噬,抑制氧化磷酸化水平,最终实现对肿瘤生长的负向调控。体内实验进一步验证,在KrasLSL-G12D/+小鼠模型中,利用腺相关病毒(AAV)在小鼠肺部过表达MAP2K6,可显著降低KRAS驱动的小鼠肺部成瘤率。本项研究不仅首次揭示了MAP2K6-BCL2L13磷酸化信号轴在细胞器互作界面上调控线粒体质量的新机制,也为肺腺癌的临床治疗提供了潜在的干预新靶点。
本研究由中国科学院广州生物医药与健康研究院、广州医科大学、广州国家实验室、中国科学院香港创新研究院再生医学与健康创新中心和中山大学肿瘤中心等多个研究组合作完成。本研究获国家重点研发项目、中国科学院、国家自然科学基金、中国科学院青年创新促进会、广东省和广州市的经费支持。广州健康院陈可实研究员、刘兴国研究员、广州医科大学第一附属医院梁文华教授和广州国家实验室董鸣研究员为该论文的共同通讯作者。广州健康院邢广锁博士为该论文的第一作者。
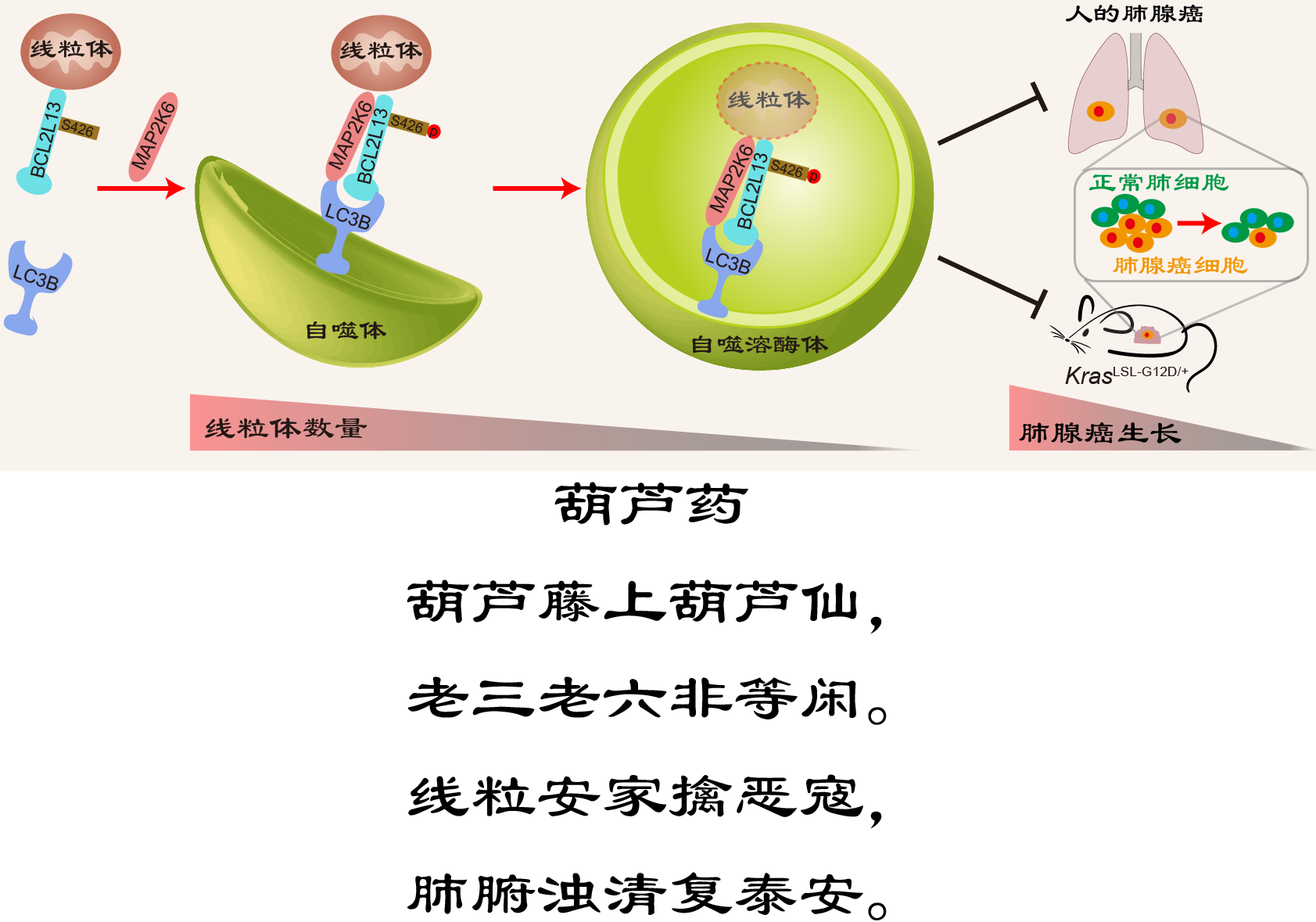
图注:将MAPK信号通路中的二级激酶MAP2K1-7比作七个葫芦娃兄弟,其中“老三”与“老六”对应MAP2K3和MAP2K6。二者定位至线粒体,通过促进线粒体自噬,有效抑制肺腺癌的发生,并保护肺组织功能,恰如诗中所述:“线粒体安家擒恶寇,肺腑浊清复泰安”。(来自刘兴国研究员的创意)
附件下载:



