

发布时间:2024-04-03
新冠病毒具有较强的免疫逃逸能力,小分子药物是抗击新冠感染的选择之一。来瑞特韦片(Leritrelvir,研究代号:RAY1216)是国内首款无需联用利托那韦靶向新冠病毒主要蛋白酶(Main protease,Mpro)的小分子化学药物,中国科学院广州生物医药与健康研究院合作对该药物抗病毒机制、抗病毒活性及药代性质进行多角度、全方位研究,揭示其多方面亮点。研究成果以“Preclinical evaluation of the SARS-CoV-2 Mpro inhibitor RAY1216 with improved pharmacokinetics compared to nirmatrelvir”为题发表在学术期刊Nature Microbiology(《自然-微生物学》)。
研究揭示RAY1216在体内外的抗病毒实验中表现出与辉瑞奈玛特韦(Nirmatrelvir (PF-07321332)相当水平的抗病毒药效。RAY1216对SARS-CoV-2多种变异株均显示出良好的抗病毒活性,半数效应剂量(EC50)均处于纳摩尔级别,能够有效抑制多种新冠变异株在Vero E6细胞中的增殖复制,显著降低病毒滴度水平。在K18-hACE2转基因小鼠模型中,来瑞特韦的治疗不仅有效地提高感染小鼠的生存保护率,也显著降低了其肺部病毒载量,减缓了由病毒感染导致的体重减轻,改善了感染肺损伤病理变化的表征。研究还利用复制子方法验证了RAY1216对于目前对PF-07321332强耐药的主蛋白酶突变体L50F+E166V仍然保持一定的抑制作用(EC50=233±4 nM)。
研究团队还在大鼠和小鼠模型上进行了来瑞特韦的药代动力学测试,在口服灌注或注射且不联用利托纳韦的情况下,实验结果证明RAY1216具有优秀的药代动力学性质。RAY1216在体内的药物血浆暴露量高于对照药物PF-07321332,体内清除率低,代谢半衰期长,其优秀的药代动力学性质表现为其在临床上的单药使用提供了有力的科学证据。
研究在原子结构和化学动力学上明确了RAY1216抑制主蛋白酶的机制。团队通过酶活抑制动力学分析测得RAY1216对SARS-CoV-2的主蛋白酶的抑制常数(Ki)为8.4 纳摩尔,药物在靶点的停留时间至少为104分钟,远长于辉瑞PF-07321332的9分钟。研究解析了RAY1216-主蛋白酶复合物的晶体结构,确证了RAY1216的酮酰胺弹头以共价方式结合在主蛋白酶催化位点145位的半胱氨酸上。相对于辉瑞PF-07321332,RAY1216与主蛋白酶的相互作用更多,抑制复合物更加稳定,使得其靶点停留时间更长,抑制更彻底。这些数据充分解释了RAY1216的抗病毒功能。
建立在以上临床前的研究数据,RAY1216完成了1-3期临床试验,在2023年3月获批以单药来瑞特韦片(商品名:乐睿灵)上市用于新冠感染的治疗。
论文通讯作者是广州医科大学附属第一医院、广州呼吸健康研究院、呼吸疾病全国重点实验室、国家呼吸系统疾病临床医学研究中心、广州实验室钟南山院士和杨子峰教授,中国科学院广州健康院熊晓犁研究员等。广东众生睿创生物科技有限公司、中山大学药学院(深圳)陈小新博士,广州医科大学附属第一医院与中国科学院广州健康院联合培养硕士生黄晓东、广州医科大学附属第一医院马钦海副研究员,美国麻省BioKin公司Petr Kuzmič博士为论文的第一作者。研究获得广州实验室陈新文研究员与陈继征研究员团队,中国科学院广州健康院刘劲松研究员与许永研究员团队等大力合作支持。该研究成果得到国家重点研发计划、国家自然科学基金、广东省自然科学基金等项目的资助。研究的蛋白结构数据在上海光源BL19U1和BL10U2线站获得,线站为蛋白晶体衍射数据的收集提供了大力的支持 。
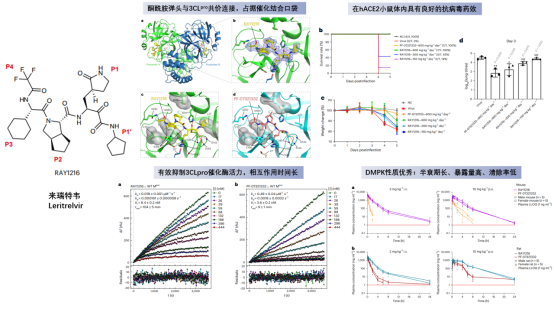
来瑞特韦的作用机制、抗病毒效果及药代动力学研究数据
附件下载:

