

发布时间:2017-12-18来源:供稿:干细胞所 吴迪
11月15日,中国科学院广州生物医药与健康研究院李鹏研究组在国际学术期刊Oncotarget上发表题为 “Defined,serum/feeder-free conditions for expansion and drug screening of primary B-acute lymphoblastic leukemia”的研究成果,揭示了MSCs(mesenchymal stem cells)促进B型急性淋巴细胞白血病(B-ALL, B Acute lymphoblastic leukemia)细胞生长的深层机制,以此确立了原代B-ALL细胞体外培养体系,建立了个性化的药物高通量筛选平台。
对化合物进行功能性筛选是B-ALL合理治疗方法发展的主要障碍。同时,由于细胞系在体外容易产生基因、表型漂移和丢失异质性,其作为药物筛选主流模型的可信性也受到了质疑。因此,解决原代细胞在体外培养和扩增困难的问题刻不容缓。
该研究发现,OP9细胞,而非OP9来源的脂肪细胞,能够促进B-ALL原代细胞的体外生长,并通过RNA-Seq分析确定了支持这些细胞在体外生长的主要成分,据此建立了一种无血清培养体系FI76V。利用此体系可在体外培养和扩增一系列临床常见的原代细胞,且保持这些细胞最初的生物学特性。同时,研究人员基于此体系建立了一种高通量药物筛选平台,对378种激酶抑制剂进行筛选后,找到能在体外有效杀伤B-ALL细胞的17种激酶抑制剂。同时,该研究也以此验证了dinaciclib和BTG226联合用药治疗B-ALL白血病的有效性。
该项目获得中科院干细胞先导、国家自然科学基金、广东省自然科学杰出青年基金等项目的资助。
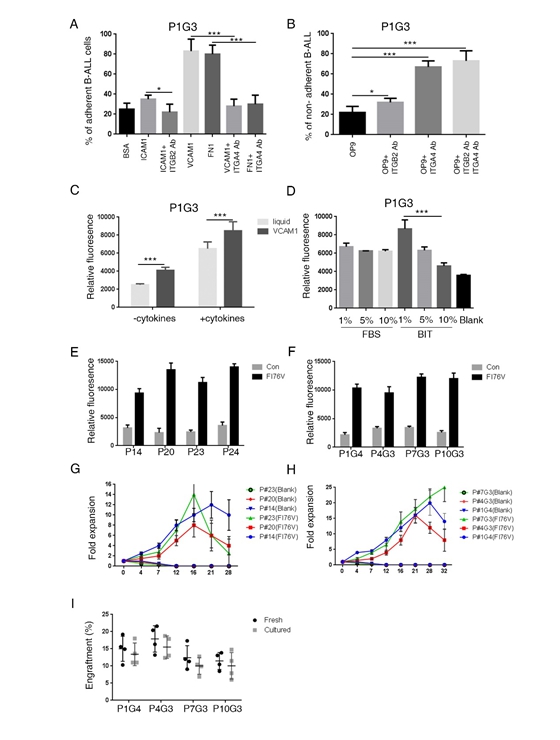
FI76V培养基能在体外有效促进B-ALL细胞的生长,同时能保持其在体内起始白血病的能力
附件下载:



