

发布时间:2024-01-19
近日,中国科学院广州生物医药与健康研究院刘晶团队在Cell & Bioscience期刊发表了题为“Epigenetic reshaping through damage: promoting cell fate transition by BrdU and IdU incorporation”的文章。该研究揭示了碱基类似物BrdU和IdU通过DNA损伤修复途径调控组蛋白乙酰化和DNA去甲基化从而促进体细胞重编程的分子作用机制,同时在多个重编程系统中验证并发现了其剂量与作用结果之间的相关性。
该研究基于实验室前期建立的化学成分明确的高效化学重编程体系(Cao et al., 2018),其中BrdU作为碱基类似物在该系统中发挥着至关重要的作用,但机制尚不明确。碱基类似物具有随机整合到基因组中的特征,其随机性如何参与精密的体细胞重编程过程,同时体细胞重编程本质是表观遗传重编程的过程,这种影响基因组的作用方式最终如何调控表观遗传重编程是该研究拟解决的关键科学问题。
研究首先发现BrdU可在化学重编程过程两个阶段发挥作用并可被IdU替代。在第一阶段即体细胞向XEN-like转变阶段,BrdU/IdU的持续处理会造成DNA的损伤累积,通过小分子干扰双链断裂的主要修复通路ATM(ataxia telangiectasia-mutated)可显著降低化学重编程的效率。XEN-like状态关键基因Gata4、Sox17、Sall4的H3K9和H3K27乙酰化会在碱基类似物处理下特异性上调。而ATM的激活伴随着磷酸化-乙酰化的级联反应,因此得出碱基类似物可通过诱导DNA损伤激活ATM信号通路造成损伤位点的乙酰化累积,从而调控基因表达。第二阶段XEN-like状态往多能性转变的过程中,DNA甲基化是主要的限制因素,碱基类似物造成的持续损伤可使新合成的DNA双链失去原有的甲基化修饰,从而起到DNA去甲基化的作用。
最后,团队进一步在转录因子介导重编程系统中验证了该机制的普遍性,并建立了以BrdU为核心的KLF4与SOX2(KS)高效体细胞重编程系统。在该系统中,BrdU仍可通过ATM信号通路激活XEN基因进而促进体细胞重编程进程,同时发现了碱基类似物在不同重编程系统的分子作用特点,并总结了其剂量与作用结果之间的相关性。
综上,研究发现BrdU/IdU可以激活DNA损伤修复途径(HRR),导致组蛋白乙酰化和全基因组DNA去甲基化增加,从而调节体细胞重编程。该研究揭示了基因组与表观遗传在体细胞重编程中的互作关系,为细胞命运转变的机制提供了新的见解。
中国科学技术大学博士研究生李闯、硕士研究生徐小朵以及广州健康院硕士研究生陈舒妍为该论文的共同第一作者。广州健康院刘晶研究员、吴昊凯峰博士和西湖大学裴端卿教授为该论文的共同通讯作者,该研究成果得到了国家重点研发计划、国家自然科学基金等项目的资助。
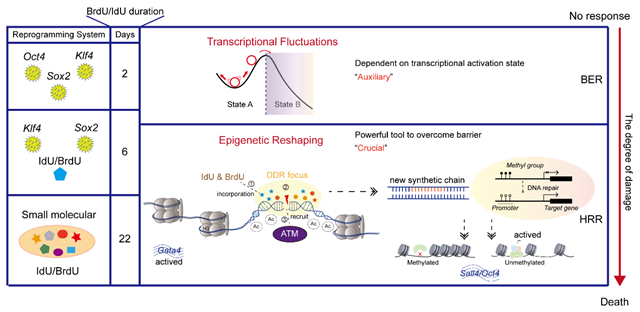
Brdu和Idu通过DNA损伤修复途径调节体细胞重编程
附件下载:

