

发布时间:2018-04-06来源:供稿:化学所 罗爽
中科院广州生物医药与健康研究院朱强研究组在钯催化的不对称亚胺基化反应研究中取得重要进展,相关研究成果发表在《美国化学会-催化》(ACS Catal. 2017, 7, 3832.)和《有机化学快报》(Org. Lett. 2018, DOI: 10.1021/acs.orglett.8b00348.)杂志上。
朱强研究员团队长期致力于杂环分子的高效的合成方法学研究。研究团队采用碳氢活化、过金属催化的异腈插入、自由基环化串联反应等策略,构建了了多个具有广泛药理活性的杂环化合物骨架。这些方法普遍具有良好的原子经济性和步骤经济性,极大地提高了它们的合成效率,为进一步的生物活性研究奠定了基础。
由于异腈与金属中心的强配位能力,异腈基团的存在直接影响了手性配体和金属中心的配位,从而降低了金属中心和配体对底物的手性控制。因此,基于异腈插入的不对称催化反应目前还很少报道,是一个非常具有挑战性的难题。在这之前的相关报道中,对映选择性(ee值)最高只有70%左右,而且也只适用于结构特殊的异腈。最近,朱强课题组在钯催化的不对称异腈插入领域取得重要突破。他们设计了官能化异腈的策略,让反应先发生异腈迁移插入,再通过手性配体调控产生手性,这样有效降低了异腈与手性配体之间的竞争,在对映选择性上实现了质的飞跃。他们和中科院上海有机化学研究所的游书力研究员合作,利用官能化异腈的策略,通过钯催化的亚胺化/不对称碳氢键活化,合成了含手性季碳的3,4-二氢异喹啉衍生物。该反应具有很高的收率(最高达99%)和ee值(最高达92%)(ACS Catalysis, 2017, 7, 3832.);随后,他们又利用类似的策略,合成了含有平面手性的吡啶并-[3,4,b]-二茂铁结构,反应的产率最高达到99%,并且ee值进一步提升,最高达99% (Org. Lett. 2018, DOI: 10.1021/acs.orglett.8b00348.)。
该项研究获得国家自然科学基金面上项目,国家自然科学基金重点项目(21532009),和中国科学院青年创新促进会人才项目资助。
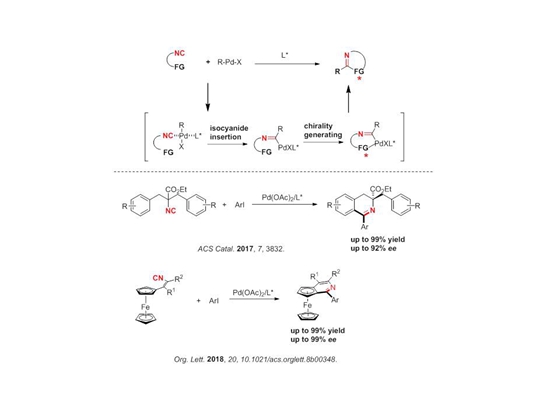
钯催化的不对称亚胺基化反应
附件下载:

