

发布时间:2015-06-23来源:黄博纯 撰稿:干细胞所 陈捷凯
6月23日,国际著名学术期刊《自然·细胞生物学》(Nature Cell Biology)在线发表了中科院广州生物医药与健康研究院裴端卿和陈捷凯实验组的研究成果“The oncogene c-Jun inhibits reprogramming”。该研究从体细胞阶段的因子出发,发现癌基因c-Jun与干细胞多能性完全不相容,而c-Jun抑制因子不仅促进重编程,还可以替代Yamanaka因子中最为核心的Oct4;在这一发现基础上结合研究组多年以来在重编程机理上的研究结果,组建了一套不包含Yamanaka因子的全新iPS细胞诱导因子。
历时8年的系统研究
经过多年研究,科学家对体细胞重编程为干细胞的过程有了一定的认识:通过强制表达多能性调控网络的核心因子,可以逐步抑制体细胞原有的特性并慢慢建立起多能性,在此过程中细胞需要克服许多表观遗传方面的障碍。然而在这些认识基础上,重编程效率仍然较低,大多数细胞仍然不会执行多能性程序,因此裴端卿和陈捷凯研究组决定对一些之前没有注意过的因子进行研究,其中就包括了可能能够强烈维持体细胞命运的核心因子。
通过这个思路,实验组发现一个非常著名的癌基因——c-Jun在表达上非常吻合:它仅在体细胞中表达,在胚胎干细胞或iPS细胞中完全不表达,而在重编程过程中观察不到明显的下降。进一步的实验发现,在胚胎干细胞中敲除c-Jun对多能性毫无影响,但成纤维细胞中敲除c-Jun会造成细胞完全无法增殖,而在胚胎干细胞强制表达c-Jun,胚胎干细胞会迅速分化并失去多能性,这些结果都提示c-Jun与多能性是完全不相容的。在体细胞重编程中的结果也完全支持这一结论,强制表达c-Jun后,Yamanaka因子介导的体细胞重编程完全被抑制,而通过多种途径抑制c-Jun,则能有效地提升iPS细胞获得的效率。
这是实验室近八年来一系列工作的结晶,单本研究中发现的c-Jun及其相关研究就做了近七年。
体细胞走向干细胞的关口
科研人员对c-Jun抑制因子做了进一步的研究,惊喜地发现c-Jun抑制因子不仅可以提升重编程效率,更可以有效替代Yamanaka因子中最为核心的因子、同时也是干细胞多能性调控网络的核心因子Oct4。这提示抑制c-Jun这个体细胞的核心因子,也能起到加入类似Oct4这样的干细胞激活因子的作用,这对目前关于体细胞重编程的认识是一个冲击。
裴端卿和陈捷凯实验组结合过去的一些原创性发现,尝试开发一套新的重编程因子。首先被选中的因子是Jhdm1b,作为维生素C提升体细胞重编程的重要下游靶因子,Jhdm1b与Oct4共表达时即可以使体细胞重编程为干细胞;其次被选中的因子是Id家族的Id1,Id家族作为BMP信号通路的下游,在无Klf4的重编程体系中能够有效地提升重编程效率。实验人员在包括c-Jun抑制因子Jdp2在内的三因子基础上进行了大量筛选和反复测试,又加入了Sall4、LRH-1和Glis1三个因子,最终确定了一套不包含Yamanaka因子的全新重编程因子组合,在这套因子组合中,Jdp2、Jhdm1b和Id1是不可或缺的,但六个因子都存在时,重编程效果比较稳定。实验还显示这套全新的重编程因子组合对一些药物的反应和Yamanaka因子有所差别,证明这套系统可能代表了一条不同的重编程路径,这对于研究重编程的机理提供了崭新的思路和模型。
癌基因也能是干细胞的“死对头”
干细胞作为一个热点概念,当前面临大量质疑,比如因为干细胞具有无限增殖的潜能,加上癌症干细胞的发现,不仅使人联想到干细胞是否具有和癌细胞一样的特征,这一问题众说纷纭。而重编程iPS细胞的Yamanaka因子中有一个著名的癌基因c-Myc,在后来的研究中,科学家又发现著名的抑癌基因通路p53、p21会抑制体细胞转化为干细胞,这些事实都提示干细胞可能和癌细胞共享一些通路,这在直觉上无疑加深了对干细胞的怀疑。c-Jun作为第一个被定义为癌基因的转录因子,正常表达时对于体细胞增殖分裂是必须的,但如果异常高表达,就有癌变的风险。增加c-Jun表达时,用于“返老还童”的体细胞确实会增殖加快,在以往多数研究中,这会对iPS细胞的形成有好处,然而c-Jun的增加却完全抑制了iPS细胞的产生,这说明癌基因并不是iPS形成的关键。
这项研究阐明了c-Jun与干细胞多能性互不相容的机理,提出了全新的重编程因子组合,为体细胞重编程的机理提供了新的思路。该研究成果由裴端卿和陈捷凯实验组合作完成,刘晶副研究员是本论文的第一作者,研究得到了来自中国科学院、国家科技部、国际自然科学基金委、广东省及广州市等多方面的经费支持。
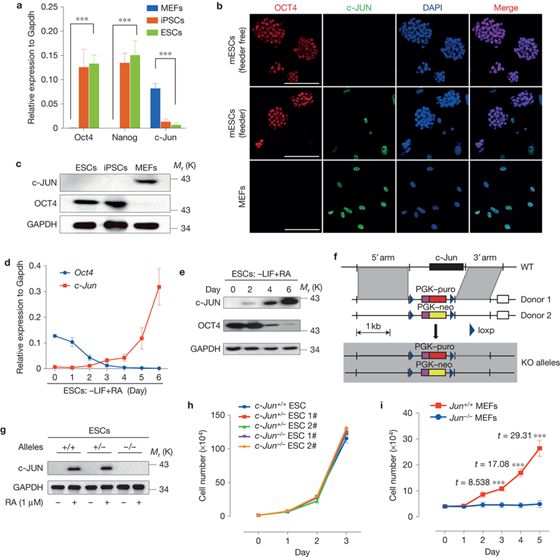
广州生物院发现全新的iPS细胞诱导因子
附件下载:

